Saegusa-Ito氧化反应
时间: 2023-05-22
作者: 百灵威
分享:
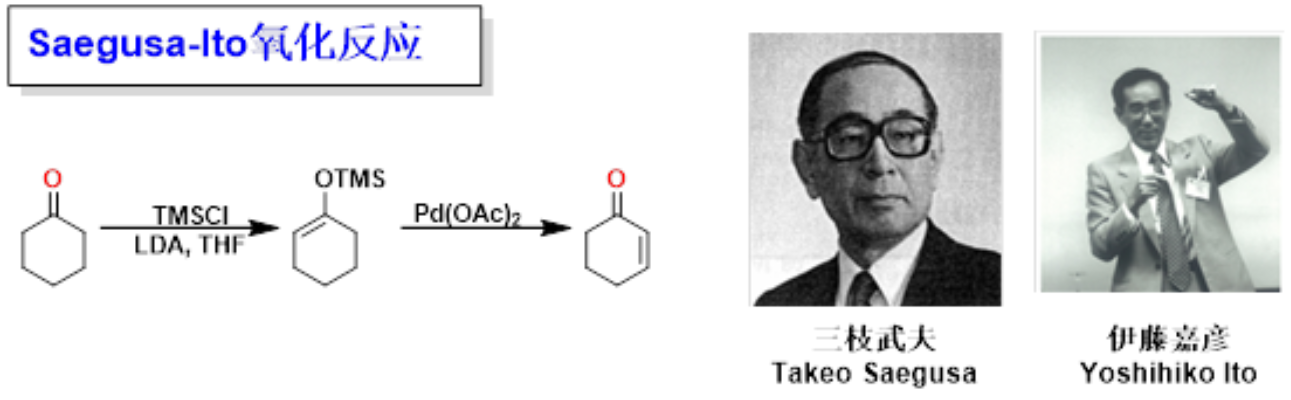
Saegusa-Ito氧化(Saegusa-Ito Oxidation reaction)是先将酮转化为相应的烯醇硅醚,然后在醋酸钯和对苯醌条件下发生区域选择性氧化获得α,β-不饱和酮的反应。
该反应由日本Kyoto University的Yoshihiko Ito(伊藤嘉彦)与Takeo Saegusa(三枝武夫)在1978年首次报道[1]。
Saegusa-Ito氧化反应条件温和,但由于该反应需要当量的醋酸钯,严重限制了其在化学合成中的应用,为了减少催化剂用量,反应被进行各种改良,如1)Larock(Richard C. Larock)改良法,DMSO的溶剂中氧气可以再生Pd(II),使得反应的醋酸钯降至催化量[2];2)二价铜替代氧化剂;3)Jiro Tsuji改良法(辻二郎)以碳酸二丙烯基酯做氧化剂[3]。
反应机理
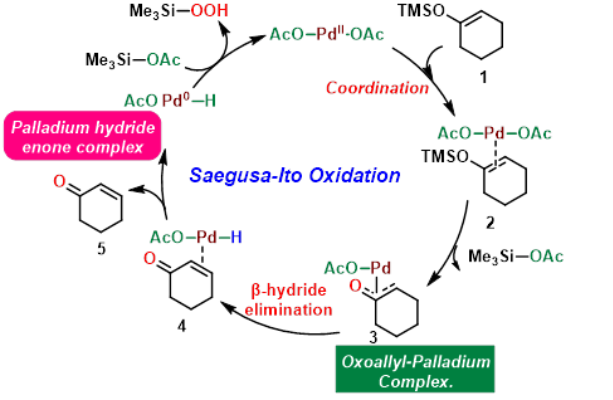
Pd(II)与1配位生成中间体2,中间体2失去TMSOAc形成氧-烯丙基钯络合物3。随后,中间体3发生β-氢消除生成钯氢-烯酮络合物4, 中间体4还原消除生成产物5、乙酸以及Pd(0)。最后,Pd(0)在氧气条件下氧化生成Pd(II),进入下一个催化循环。值得注意的是,β-氢消除步骤[4]是一个存在化学平衡的可逆反应,所以对于非环状的底物,反应会选择性地生成E-双键构型的热力学产物。反应实例
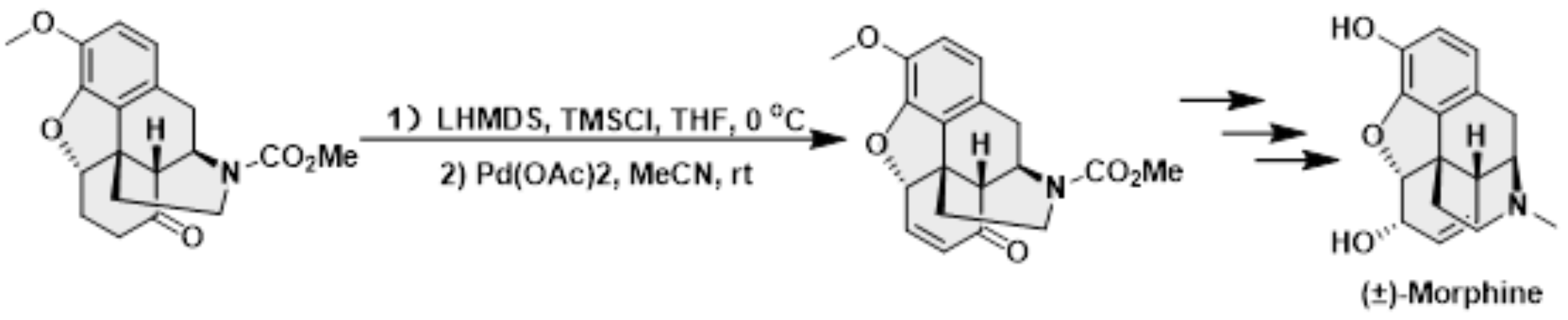
(±)-Morphine的全合成[5]
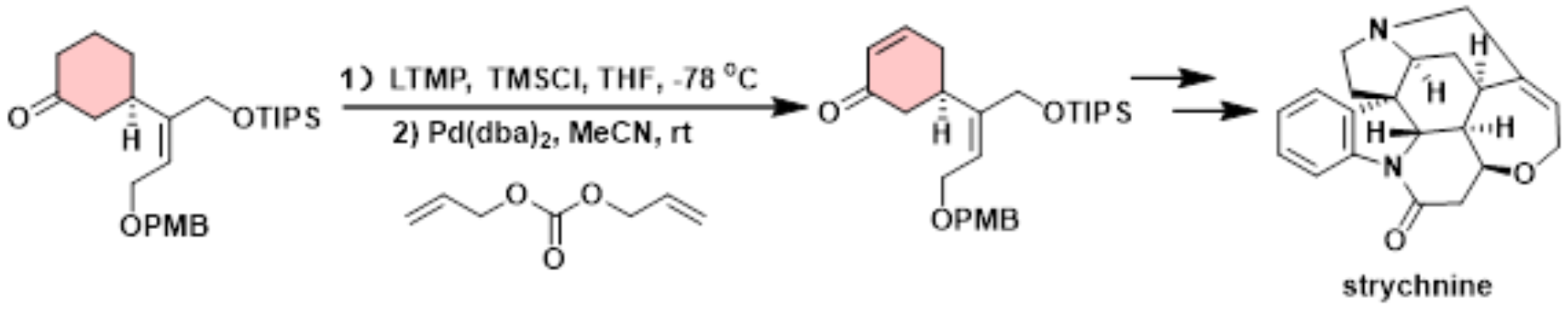
Strychnine的全合成[6]
参考文献
- T. Hirao, T. Masunaga, Y. Ohshiro, T. Agawa, J. Org. Chem. 1981, 46, 3745. Y. Ito, T. Hirao, T. Saegusa, J. Org. Chem. 1978, 43, 1011-1013. doi: 10.1021/jo00399a052
- R. C. Larock, T. R. Hightower, G. A. Kraus, P. Hahn, D. Zheng, Tetrahedron Lett. 1995, 36, 2423-2426. doi: 10.1016/0040-4039(95)00306-W
- J. Tsuji, I. Minami, I. Shimizu, Tetrahedron Lett. 1983, 24, 5635-5638.doi: 10.1016/S0040-4039(00)94160-1
- Oxidation Archived 2011-03-12 at the Wayback Machine, Chem 215 lecture notes
- K. Uchida, S. Yokoshima, T. Kan, T. Fukuyama, Org. Lett. 2006, 8, 5311-5313. doi: 10.1021/ol062112m.
- T. Ohshima, Y. Xu, R. Takita, S. Shimizu, D. Zhong, M. Shibasaki, J. Am. Chem. Soc. 2002, 124, 14546-14547.doi: 10.1021/ja028457r.
相关化合物
| 品名 | CAS | 货号 |
|---|---|---|
| Palladium(II) acetate, min. 98% (99.9+%-Pd) 醋酸钯(II), (99.9+%-Pd) | 3375-31-3 | 46-1780 |
| n-Butyllithium, 1.6 M solution in hexanes, J&KSeal 正丁基锂 , 1.6 M 己烷溶液, J&KSeal瓶 | 109-72-8 | 274232 |
| Dimethyl sulfoxide, 99% 二甲基亚砜 , 99% | 67-68-5 | 984549 |
| Chlorotrimethylsilane, 99%, J&KSeal 三甲基氯硅烷 , 99%, J&KSeal瓶 | 75-77-4 | 458784 |
相关产品请点击查看
百灵威有机锂系列产品相关阅读
百灵威FM库存管理系统-免费试用 百灵威FM电子实验记录本-免费试用 合成百宝箱——人名反应大汇总百灵威超干溶剂