冯氏配体—用于[n+2]环加成反应
环加成反应是两个或多个不饱和化合物(或同一化合物的不同部分)结合生成环状化合物并伴随有系统总键级数减少的化学反应。它是生成许多环状化合物的重要方法。
冯小明院士团队设计的 N,N'-双氧化合物(即冯氏配体),突破了对配体刚性骨架的传统要求,像“双节棍”一样刚柔并济,通过控制化学物质在反应中的相遇方式,保证它们按照预期的方式结合。
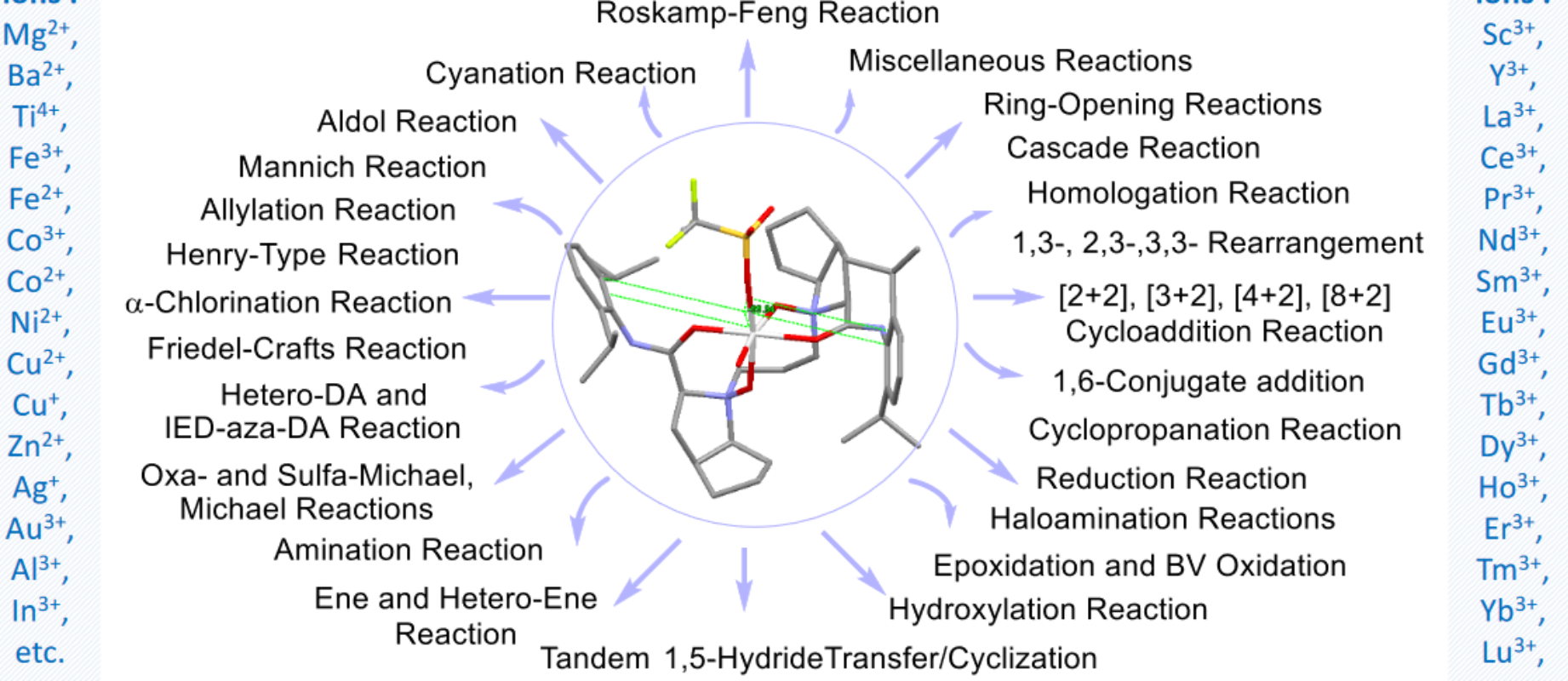
冯氏配体作为一类重要的配体,可用于[3+2], [4+2], [8+2]等不对称环加成反应中,高效合成多种手性环状化合物。
不对称[8+2]环加成
以手性N,N′-二氧化物(冯氏配体)L–Ni(II) 复合物为催化剂,以氮杂七烯与亚烷基丙二酸酯为底物,在温和条件下实现不对称[8+2]环加成反应,生产官能化的环庚三烯稠合吡咯衍生物。该反应的产率高(达到99%),非对映选择性(>95:5 dr)和对映选择性(91–97 % ee )好。
![不对称[8+2]环加成<sup>[1]</sup>](https://shop.jkchemical.com/res/2-2818.png)
不对称[3+2]环加成
四氢吲哚嗪的多样化转化
以高效的方式对结构和功能相似或不同的小分子集合进行对映选择性多样化合成是一项极具挑战性的任务。
研究者首先使用吡啶叶立德与烯酮进行非对映选择性和对映选择性[3+2] 环加成,随后进行多样化的连续转化。手性N,N'-二氧化物-稀土金属配合物能够在外消旋体形成的强背景反应中原位生成光学活性的四氢吲哚。通过精心设计的连续转化,包括重芳氧化和光活性 aza-Norrish II 重排,四氢吲哚中间体最终被转化为包括3-芳基吲哚衍生物和二碳官能化的1,5-二羰基化合物等。不仅如此,四立体中心四氢吲哚中间体的立体化学可以有效地转化为 3-芳基吲哚和邻位吡啶基和芳基取代的 1,5-二酮中的轴向手性。
![四氢吲哚嗪的多样化转化<sup>[2]</sup>](https://shop.jkchemical.com/res/2-2819.png)
环外烯醇醚的催化不对称 [3+2] 环加成
通过催化不对称[3+2] 环外烯醇醚与对位醌环加成,高效合成了手性苯并环化螺酮。该转化由手性N, N′-二氧化物/Tm(III)复合物作为路易斯酸催化剂实现,并以良好的产率(高达 99%)和对映选择性(高达 98% ee)得到一系列对映体富集的苯并环化螺酮衍生物。
![环外烯醇醚的催化不对称 [3+2] 环加成<sup>[3]</sup>](https://shop.jkchemical.com/res/2-2820.png)
不对称[4+2] 环加成
以手性 N,N'-二氧化物/镍 (II) 复合物作为高效催化剂,亚甲基吲哚酮与 1,3-二烯基氨基甲酸酯和 1,2-二氢吡啶实现了高效的非对称 Diels-Alder 反应,生成新型螺环吲哚-环己酰胺,产率高达 99%,>95 : 5 dr,ee 高达 99%。
![不对称[4+2] 环加成<sup>[4]</sup>](https://shop.jkchemical.com/res/2-2822.png)
冯氏配体
| 品名 | CAS | 货号 |
|---|---|---|
| NO-Feng-PDiPPRa, L-RaPr2, 95% NO-冯-PDiPPRa | 1005495-74-8 | 1595287 |
| NO-Feng-PDEtPPr, L-PrEt2, 95% NO-冯-PDEtPPr | 1313215-45-0 | 2699012 |
| NO-Feng-PTMPPP, L-PiMe3, 99% NO-冯-PTMPPP | 1310585-10-4 | 1595286 |
金属盐
| 品名 | CAS | 货号 |
|---|---|---|
| Nickel(II) tetrafluoroborate hexahydrate, 99% 四氟硼酸镍(II)六水合物 | 15684-36-3 | 93-2841 |
| Thulium(III) trifluoromethanesulfonate, 98% 三氟甲烷磺酸铥(III) | 141478-68-4 | 270959 |
溶剂
| 品名 | CAS | 货号 |
|---|---|---|
| 1,2-Dichloroethane, 99% 1,2-二氯乙烷 | 107-06-2 | 353972 危化品 |
| p-Xylene, 99%, SuperDry, with molecular sieves, water≤50 ppm, J&Kseal 对二甲苯 | 106-42-3 | 980760 危化品 |
参考文献
- Xie, M. S. Angew. Chem. Int. Ed. 2013, 52, 5604.
- Zhang, D. J. Am. Chem. Soc. 2020, 142, 15975.
- Zhang, F. C. Precis. Chem. 2023, 1, 423.
- Zhou, Y, H. Chem. Commun. 2017, 53, 2060.
推荐阅读
冯小明院士科研成果 | 冯氏手性双氮氧配体&催化剂——广谱性强、立体选择性好手性配体——品种齐全,选择性好,更有最新科研成果供应